한미사이언스 지분 50% 매각설...임종윤 측 "사실 무근"
2024-05-10
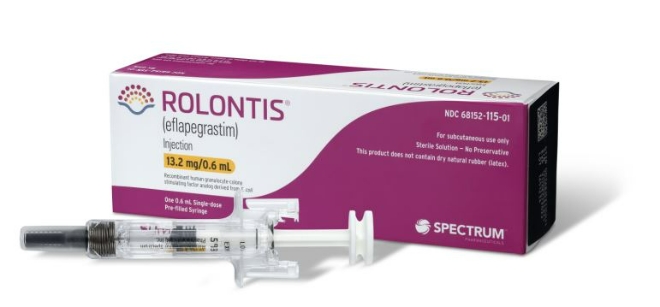
롤론티스는 한미약품이 개발한 장기지속형 호중구감소증 치료제로, FDA는 처방의약품신청자수수료법(PDUFA)에 따라 오는 9월9일 이전에 최종 허가 여부를 결정할 예정이다. 스펙트럼은 항암화학요법을 받는 비골수성 악성종양 환자의 호중구감소증으로 인한 감염 위험을 낮출 것으로 기대하고 있다.
권세창 한미약품 대표이사(사장)는 "롤론티스의 FDA 허가를 위한 마지막 관문에 공식적으로 진입했다"며 "롤론티스의 성공적인 시판 승인을 위해 파트너사인 스펙트럼과 긴밀히 협력해 나가겠다"고 말했다.
황성완 기자 skwsb@smartfn.co.kr
















댓글
(0)